Радионуклидная оценка кровотока в системе легочной артерии и параметров сократимости правого желудочка у пациентов со стенозом митрального клапана
К.В. Завадовский, А.В. Евтушенко, Ю.Б. Лишманов
ФГБУ НИИ кардиологии Сибирского отделения РАМН, лаборатория радионуклидных методов исследования, отделение сердечно-сосудистой хирургии, г. Томск, Россия
634012, г. Томск, ул. Киевская 111а
Тел: 3822-558298; факс: 3822-555057; e-mail:
РЕФЕРАТ: Цель работы – определить возможности радионуклидной ангиопульмонографии и томовентрикулографиии в оценке легочной гемодинамики и функционального состояния правых отделов сердца у пациентов со стенозом митрального клапана. В исследование были включены 26 больных со стенозом митрального клапана. Всем пациентам была выполнена радионуклидная ангиопульмоно- и томовентрикулография. У пациентов со стенозом МК наблюдалось расширение волн, соответствующих «зонам интереса» обоих желудочков и легкого, достоверное замедление легочного кровотока и снижение сократительной функции правого желудочка. По результатам многофакторного регрессионного анализа разработана модель прогнозирования восстановления сократительной функции правого желудочка после коррекции порока.
КЛЮЧЕВЫЕ СЛОВА: стеноз митрального клапана, радионуклидная томовентрикулография, легочный кровоток, правый желудочек.
Актуальность
Клапанные пороки составляют 20-25% (а среди лиц молодого возраста – до 90%) от общего числа всех структурных поражений сердца, [1, 2]. При этом наиболее часто поражается митральный клапан (МК), изолированный порок которого встречается в 24,8-70,0% случаев [3, 2].
Важными звеньями гемодинамических расстройств при стенозе митрального клапана (СМК) являются функциональные и структурные изменения легочных сосудов, а также дисфункция и недостаточность правого желудочка (ПЖ) [3]. Об этом же свидетельствуют и результаты исследований de Groote P. [4], в которых было показано, что именно сократительная дисфункция ПЖ предопределяет клиническую тяжесть состояния пациентов при рассматриваемой патологии. В работе Pande S. et al. [5] показано, что снижение давления в легочной артерии само по себе не является предиктором послеоперационного улучшения сердечной гемодинамики у больных со стенозом митрального клапана ревматической этиологии. В контексте изложенного можно с уверенностью сказать, что изучение структурно-функционального состояния правых отделов сердца является актуальным вопросом современной лучевой диагностики. Однако большинство используемых в рутинной клинической практике методов визуализации имеют ряд ограничений.
Так, трансторакальная эхокардиография, наиболее часто используемая для оценки гемодинамики сердца при митральных пороках, не позволяет адекватно оценить объемы правого желудочка, что связано, во-первых, с определенными математическими допущениями при использованием модели Симпсона [6], и, во-вторых, с загрудинным расположение свободной стенки правого желудочка, что зачастую определяет сложности ее ультразвуковой визуализации [7, 8].
Магнитно-резонансная томография, применяемая как для диагностики дисфункции ПЖ [9], так и для оценки легочного кровотока [10], противопоказана пациентам с электрокардиостимуляторами, которые часто имплантируются после коррекции пороков митрального клапана, осложненных фибрилляцией предсердий [11]. Кроме того, среди исследователей до сих пор нет единства мнений относительно используемых для визуализации сердца импульсных последовательностей [12].
Альтернативным подходом к оценке легочной гемодинамики и функционального состояния правого желудочка может быть использование методов радионуклидной индикации – радионуклидной ангиопульмонографии (РАПГ) и томовентрикулографии (РТВГ). В то же время в мировой и отечественной литературе практически не встречается работ, посвященных методологии проведения данных исследований и интерпретации полученных результатов у пациентов с митральным стенозом.
Цель – определить возможности радионуклидной ангиопульмонографии и томовентрикулографиии в оценке легочной гемодинамики и функционального состояния правых отделов сердца у пациентов со стенозом митрального клапана.
Материалы и методы
В исследование были включены 26 больных (18 женщин и 8 мужчин в возрасте от 27 до 74 (54,2±8,22) лет, находившихся на госпитализации в отделении сердечно-сосудистой хирургии (рук. – проф. В.М. Шипулин) ФГБУ НИИ кардиологии СО РАМН в 2009-2011 гг. У всех пациентов был диагностирован порок митрального клапана ревматической этиологии («чистый» стеноз или его преобладание) с индексом площади левого атриовентрикулярного клапана менее 0,7 см2/м2. Диагноз стеноза митрального клапана устанавливался на основании клинических наблюдений, результатов лабораторных исследований, ЭхоКГ, рентгенологического обследования, контрастной ангиокардиографии и зондирования полостей сердца.
Среднее давление в легочной артерии по данным ЭхоКГ составило 50,66±10,76 мм рт.ст. На момент поступления у всех пациентов была зарегистрирована фибрилляция предсердий, а также сердечная недостаточность III и выше функционального класса (ФК) по классификации Нью-Йоркской ассоциации кардиологов (NYHA). Девятнадцать больных были обследованы до и после коррекции митрального порока. Данным пациентам выполняли протезирование митрального клапана механическим двустворчатым протезом «Мединж-2» с частичным сохранением задней створки и подклапанных структур.
Группу контроля составили 15 больных ИБС сопоставимого (56,3±8,3 года) возраста, страдающих стенокардией напряжения II ФК, хронической сердечной недостаточностью 1-2 стадии, имеющих II функциональный класс по NYHA. У данных пациентов по результатам полного клинико-инструментального исследования были исключены заболевания и патологические процессы, приводящие к явлениям правожелудочковой недостаточности.
За 2-3 суток до и через 3-4 недели после хирургической коррекции митрального порока все пациенты были обследованы методом РАПГ и РТВГ на томографической двудетекторной гамма-камере «Philips-Forte», оснащенной параллельными высокоразрешающими коллиматорами (RembrandtTM) и настройкой окна дифференциального дискриминатора на энергетический пик 140±10% КэВ. В качестве радиофармпрепарата (РФП) для РАПГ использовали стерильный раствор 99mTc-натрия пертехнетата, для РТВГ – эритроциты, меченные in vivo технецием-99m. При выполнении РТВГ детектор гамма-камеры устанавливали в левую передне-косую проекцию и в момент инъекции РФП начинали динамическую запись со скоростью 0,5 кадров/с, продолжительность сбора данных составляла 100 сек. При выполнении РТВГ с углом вращения 180° детекторы гамма-камеры устанавливали в положение 90° по отношению друг к другу. Поворот детекторов происходил в автоматическом пошаговом режиме с углом смещения 2,8° по нециркулярной орбите – с максимальным приближением детекторов к поверхности тела пациента. Синхронизированная с ЭКГ запись информации была выполнена в матрицу 64×64 пиксела в 64 проекциях с экспозицией 45 секунд на кадр. Представительный сердечный цикл был разделен на 16 кадров. Эквивалентная доза составила 0,0021 мЗв/МБк, что не превышало предельно допустимого уровня для данной категории пациентов.
С использованием специализированной программы JetStream® Workspace Release 3.0 (Philips, Нидерланды) вычисляли основные показатели легочной гемодинамики:
- ТПНП – период полунакопления индикатора в правых отделах сердца;
- ТМП – время достижения максимума волны правого желудочка;
- ТПР – константа опорожнения правых отделов сердца;
- Т1/2ПЖ – период полуопорожнения правого желудочка;
- ТПНЛ – период полунакопления индикатора в левых отделах сердца;
- ТМЛ – время достижения максимума волны ЛЖ;
- ТЛЕВ – константа опорожнения левого желудочка;
- Т1/2ЛЖ – период полуопорожнения левого желудочка;
- ТЛЕГ – среднее время циркуляции крови в малом круге;
- ТАМ – модальное артериальное время;
- ТВМ – модальное венозное время;
- ТПСЛ – минимальное время циркуляции крови по полостям правой половины сердца и легким;
- ТМИН – минимальное время циркуляции крови в легких;
- ТАМН – артериальное минимальное время;
- ТВМК – минимальное венозное время в малом круге кровообращения;
- Т1/2ЛС – период полуопорожнения легочного ствола.
При помощи специализированной программы Quantitative Blood Pool SPECT 2.0 (Cedars-Sinai Medical Center, США) вычисляли следующие показатели функционального состояния правого желудочка: конечно-систолический (КДО), конечно-диастолический (КСО) и ударный (УО) объемы, фракцию выброса (ФВ), максимальную скорость изгнания (МСИ) и наполнения (МСН), среднее время наполнения за 1/3 диастолы (СВН/3), время максимума наполнения (ВМН, мс). В эти же сроки методом трансторакальной ЭХО-КГ всем пациентам определяли передне-задний и поперечный размеры правого желудочка.
Статистическую обработку результатов выполняли при помощи программы MYSTST 12 Version (SYSTAT Software, Inc, 2007). Данные представлены в виде среднего арифметического ± стандартное отклонение (M±SD). Полученные данные не подчинялись закону нормального распределения (по критерию Колмагорова-Смирнова), в связи с чем достоверность межгрупповых различий оценивали по непараметрическому критерию Wilcoxon и Mann-Whitney, взаимосвязь – по критерию Pirson.
Результаты и обсуждение
У пациентов со стенозом МК кривые РАПГ визуально отличались от таковых, полученных у лиц группы сравнения (рис. 1). В частности, наблюдалось расширение волн, соответствующих «зонам интереса» обоих желудочков и легкого, а также увеличение расстояния между пиками волн правого и левого желудочков сердца. Кроме того, отмечалось снижение крутизны восходящих и нисходящих отрезков динамических кривых «активность-время» левого и правого желудочков.
Представленная характеристика кривых РАПГ позволяет говорить о более низкой скорости поступления РФП в правые и левые отделы сердца больных с митральным стенозом, а также о замедлении времени транзита радиоактивного болюса по артериальному и венозному звеньям легочной микроциркуляции.
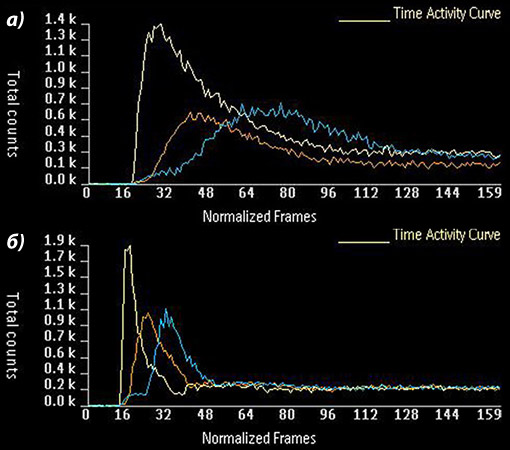
Рисунок 1. Кривые РАПГ у пациента со стенозом МК (а) и группы сравнения (б).
Волна с области ПЖ – бежевый цвет; с области легкого – оранжевый; с области ЛЖ – синий.
У пациента со стенозом МК имеет место увеличение продолжительности
и снижение крутизны восходящих и нисходящих отрезков кривых РАПГ.
Нарушения легочной гемодинамики в условиях стеноза МК, выявленные нами при визуальном анализе кривых РАПГ, подтверждались достоверными изменениями временных индексов транзита радиоактивного болюса через сосуды малого круга кровообращения. Так, при сравнительном межгрупповом анализе количественных показателей РАПГ у пациентов со стенозом МК в наибольшей степени были увеличены значения ТПНЛ и ТМЛ (табл. 1), отражающие, как известно [13], скорость поступления РФП в левые отделы сердца. Интервалы времени, характеризующие кровоток в посткапиллярном звене сосудистого русла легких (ТВМ, ТВМК), также были достоверно увеличены в группе пациентов со стенозом МК по отношению к контрольной выборке. Указанные изменения отражают развитие гипертензии в левом предсердии и легочных венах у пациентов со стенозом МК.
Сцинтиграфическим проявлением легочной гипертензии (ЛГ), обусловленной спазмом легочных артериол (рефлекс Китаева) у больных с митральным стенозом, явилось увеличение ТАМ, ТЛЕГ и Т1/2ЛС, характеризующих замедление кровотока по сосудам легких и удлинение времени эвакуации РФП из легочного ствола.
Таким образом, можно говорить, что комплекс показателей РАПГ позволяет в полной мере оценить нарушения гемодинамики МК при легочной гипертензии, обусловленной стенозом МК.
Таблица 1. Сравнительный межгрупповой анализ состояния легочной гемодинамики у пациентов со стенозом митрального клапана и в группе сравнения (M±SD)
| Показатель РАПГ | Пациенты со стенозом МК до коррекции порока (n=26) |
Пациенты группы сравнения (n=15) |
Mann-Whitney test |
|---|---|---|---|
| ТПНП, с | 2,33±1,14 | 1,31±0,54 | 0,000407 |
| ТМП, с | 5,25±3,22 | 2,57±1,06 | 0,000164 |
| ТПР, с–1 | 0,15±1,12 | 0,38±0,19 | 0,000007 |
| Т1/2ПЖ, с | 6,86±4,4 | 2,41±1,53 | 0,000008 |
| ТПНЛ, с | 4,92±2,57 | 2,07±0,36 | 0,000000 |
| ТМЛ, с | 12,10±7,08 | 5,15±0,96 | 0,000003 |
| ТЛЕВ, с–1 | 0,07±0,04 | 0,14±0,03 | 0,000001 |
| Т1/2ЛЖ, с | 16,26±14,75 | 4,93±1,18 | 0,000001 |
| ТЛЕГ, с | 14,47±3,3 | 7,80±1,48 | 0,000009 |
| ТАМ, с | 6,48±4,23 | 3,90±0,61 | 0,000726 |
| ТВМ, с | 8,01±4,7 | 3,90±1,05 | 0,000004 |
| ТПСЛ, с | 7,64±3,61 | 5,21±1,05 | 0,000352 |
| ТМИН, с | 3,57±1,48 | 2,64±0,97 | 0,002137 |
| ТАМН, с | 2,63±1,34 | 1,46±0,53 | 0,000351 |
| ТВМК, с | 9,38±5,36 | 5,01±1,12 | 0,000102 |
| Т1/2ЛС, с | 12,10±11,86 | 2,73±2,09 | 0,000001 |
Примечание: МК – митральный клапан; ТПНП – период полунакопления индикатора в правых отделах сердца; ТМП – время достижения максимума волны правого желудочка; ТПР – константа опорожнения правых отделов сердца; Т1/2ПЖ – период полуопорожнения правого желудочка; ТПНЛ – период полунакопления индикатора в левых отделах сердца; ТМЛ – время достижения максимума волны ЛЖ; ТЛЕВ – константа опорожнения левого желудочка; Т1/2ЛЖ – период полуопорожнения левого желудочка; ТЛЕГ – среднее время циркуляции крови в малом круге; ТАМ – модальное артериальное время; ТВМ – модальное венозное время; ТПСЛ – минимальное время циркуляции крови по полостям правой половины сердца и легким; ТМИН – минимальное время циркуляции крови в легких; ТАМН – артериальное минимальное время; ТВМК – минимальное венозное время в малом круге кровообращения; Т1/2ЛС – период полуопорожнения легочного ствола.
У больных с пороками митрального клапана наблюдалась выраженная дисфункция ПЖ, на что указывали статистически значимо уменьшенные величины его фракции выброса, максимальной и средней скоростей изгнания, ударного объема и превышение конечно-систолического объема по отношению к пациентам из группы сравнения (табл. 2).
Ударный объем, ФВ и МСИ правого желудочка являются показателями, характеризующими функцию изгнания, следовательно, более низкие их значения у лиц с пороками МК можно объяснить увеличенной постнагрузкой на ПЖ за счет гипертензии в малом круге кровообращения. Более низкая ССН/3 правого желудочка у таких пациентов также связана, на наш взгляд, с легочной гипертензией, приводящей к повышению конечно-систолического давления. Подтверждают это предположение и повышенное систолическое давление в ПЖ (50,66±10,76 мм рт.ст.), и более высокие значения КСО ПЖ, а также тесная корреляция между значениями КСО ПЖ и ССН/3 ПЖ (r=–0,74, p=0,001).
Таблица 2. Сравнительный межгрупповой анализ показателей РТВГ у больных
со стенозами митрального клапана и пациентов группы сравнения (M±SD)
| Показатели | Группа сравнения (n=15) |
Пациенты со стенозом МК (n=26) |
Mann-Whitney test (1 vs 2) |
|---|---|---|---|
| 1 | 2 | ||
| КДО, мл | 168,54±23,52 | 172±46,61 | 0,07 |
| КСО, мл | 76,18±20,52 | 100,37±34,21 | 0,046 |
| УО, мл | 93,38±15,66 | 69,3±27,79 | 0,00003 |
| ФВ, % | 53,84±8,63 | 40,88±10,94 | 0,03 |
| МСИ, КДО/с | -2,78±0,79 | -1,97±0,43 | 0,001 |
| МСН, КДО/с | 2,02±0,74 | 1,84±0,6 | 0,23 |
| ССН/3, КДО/с | 1,41±0,52 | 1,05±0,37 | 0,008 |
| ВМН, мс | 153,9±43,10 | 200,44±130,7 | 0,73 |
Примечание: КДО – конечно-диастолический объем; КСО – конечно-систолический объем; УО – ударный объем; ФВ – фракция выброса; МСИ – максимальная скорость изгнания; МСН – максимальная скорость наполнения; ССН/3 средняя скорость наполнения за 1/3 диастолы; ВМН – время максимального наполнения желудочка; ВЖД – внутрижелудочковая диссинхрония; МЖД – межжелудочковая диссинхрония.
Результаты РАПГ, представленные в табл. 3, свидетельствуют о том, что после коррекции стеноза МК происходило достоверное ускорение легочного кровотока, отражающее снижение давления в легочной артерии. При этом наиболее выраженным было ускорение пассажа РФП через венозное звено легочной микроциркуляции (ТВМ) и снижение времени достижении максимума волны левого желудочка (ТМЛ), обусловленное устранением препятствия току крови из левого предсердия в левый желудочек.
Таблица 3. Сравнительный внутригрупповой анализ влияния коррекции стеноза митрального клапана на радионуклидные показатели легочной гемодинамики (M±SD)
| Показатели | Пациенты со стенозом МК до коррекции порока (n=19) |
Пациенты со стенозом МК после коррекции порока (n=19) |
Wilcoxon test |
|---|---|---|---|
| ТПНП, с | 2,33±1,14 | 1,85±0,87 | 0,12 |
| ТМП, с | 5,25±3,22 | 3,79±1,84 | 0,04 |
| ТПР, с-1 | 0,15±0,12 | 0,21±0,11 | 0,007 |
| Т1/2ПЖ, с | 6,86 4,4 | 4,68 3,64 | 0,026 |
| ТПНЛ, с | 4,92±2,57 | 3,58±1,59 | 0,007 |
| ТМЛ, с | 12,1±7,08 | 8,24±3,49 | 0,002 |
| ТЛЕВ, с-1 | 0,07±0,04 | 0,09±0,04 | 0,005 |
| Т1/2ЛЖ, с | 16,26±10,75 | 9,23±5,36 | 0,007 |
| ТЛЕГ, с | 14,47±8,3 | 10,59±3,71 | 0,0006 |
| ТАМ, с | 4,48±4,23 | 4,63±1,71 | 0,012 |
| ТВМ, с | 8,07±4,7 | 5,95±2,6 | 0,002 |
| ТПСЛ, с | 7,64±3,61 | 6,13±1,74 | 0,008 |
| ТМИН, с | 3,57±2,48 | 2,94±1,37 | 0,02 |
| ТАМН, с | 2,63±1,39 | 2,09±0,94 | 0,01 |
| ТВМК, с | 9,38±5,36 | 6,32±2,38 | 0,01 |
| Т1/2ЛС, с | 12,1±11,86 | 7,37±4,82 | 0,01 |
Примечание: МК – митральный клапан; ТПНП – период полунакопления индикатора в правых отделах сердца; ТМП – время достижения максимума волны правого желудочка; ТПР – константа опорожнения правых отделов сердца; Т1/2ПЖ – период полуопорожнения правого желудочка; ТПНЛ – период полунакопления индикатора в левых отделах сердца; ТМЛ – время достижения максимума волны ЛЖ; ТЛЕВ – константа опорожнения левого желудочка; Т1/2ЛЖ – период полуопорожнения левого желудочка; ТЛЕГ – среднее время циркуляции крови в малом круге; ТАМ – модальное артериальное время; ТВМ – модальное венозное время; ТПСЛ – минимальное время циркуляции крови по полостям правой половины сердца и легким; ТМИН – минимальное время циркуляции крови в легких; ТАМН – артериальное минимальное время; ТВМК – минимальное венозное время в малом круге кровообращения; Т1/2ЛС – период полуопорожнения легочного ствола.
Как следует из табл. 4, коррекция порока реализовалась статистически значимым уменьшением конечно-систолического объема и увеличением как максимальной скорости изгнания, так и фракции выброса правого желудочка. Указанные изменения внутрисердечной гемодинамики объясняются устранением первого (суженное митральное отверстие) и второго (обусловленный рефлексом Китаева спазм легочных артериол) гемодинамических барьеров с уменьшением в связи с этим постнагрузки на правый желудочек. Устранение второго барьера подтверждается и данными трансторакальной ЭхоКГ (достоверное снижение давления в правом желудочке с 50,66±10,76 до 36,8±12,26 мм рт.ст., p=0,002).
Таблица 4. Сравнительный внутригрупповой анализ влияния коррекции стеноза митрального клапана на радионуклидные показатели правых отделов сердца (M±SD)
| Показатели | Пациенты со стенозом МК до коррекции порока (n=19) |
Пациенты со стенозом МК после коррекции порока (n=19) |
Wilcoxon test (1 vs 2) |
|---|---|---|---|
| 1 | 2 | ||
| КДО, мл | 156,93±34,66 | 153,08±31,16 | 0,64 |
| КСО, мл | 99,66±36,46 | 87,58±28,51 | 0,04 |
| УО, мл | 57,26±16,06 | 65,33±15,99 | 0,17 |
| ФВ, % | 37,66±11,94 | 43,5±11,12 | 0,005 |
| МСИ, КДО/с | –1,72±0,63 | –2,20±0,62 | 0,01 |
| МСН, КДО/с | 1,69±0,71 | 1,88±0,47 | 0,64 |
| ССН/3, КДО/с | 0,97±0,4 | 1,09±0,28 | 0,38 |
| ВМН, мс | 189,4±136,36 | 149,83±32,53 | 0,28 |
Примечание: КДО – конечно-диастолический объем; КСО – конечно-систолический объем; УО – ударный объем; ФВ – фракция выброса; МСИ – максимальная скорость изгнания; МСН – максимальная скорость наполнения; ССН/3 средняя скорость наполнения за 1/3 диастолы; ВМН – время максимального наполнения желудочка; ВЖД – внутрижелудочковая диссинхрония; МЖД – межжелудочковая диссинхрония; ПП (trans.) – поперечный размер правого предсердия; ПП (sag.) – сагиттальный размер правого предсердия; ПП (front) – фронтальный размер правого предсердия.
Как известно, состояние сократительной функции ПЖ является наиболее значимым независимым предиктором клинического исхода заболевания при клапанной патологии [14]. В нашем исследовании для определения прогноза состояния правого желудочка после коррекции порока пациенты были разделены на две подгруппы:
- Пациенты (n=13), у которых функция ПЖ после коррекции СМК была удовлетворительной (ФВ ПЖ ≥40%)
- Пациенты (n=6), у которых после операции функция ПЖ была снижена (ФВ ПЖ <40%)
Значения СДПЖ у больных указанных подгрупп после оперативного вмешательства достоверно не различались. Кроме того, мы не выявили достоверной корреляции между СДПЖ правого желудочка до операции (по данным допплер-ЭхоКГ) и сцинтиграфическими показателями функционального состояния ПЖ после коррекции порока. В этом аспекте полученные нами данные согласуются с результатами работы Pande S. [5], указывающими, что основные эхокардиографические признаки дисфункции правого желудочка (систолическое движение кольца трикуспидального клапана, укорочение кольца трикуспидального клапана и укорочение длинной оси ПЖ) не всегда зависят от величины систолического давления в его полости, поскольку функциональное состояние правых отделов сердца зависит от преморбидного фона, выраженности гипертрофии миокарда ПЖ, его ишемии, межжелудочкового взаимодействия и других факторов. В свете сказанного мы не считаем целесообразным использовать СДПЖ в качестве прогностического критерия нормализации функции ПЖ после коррекции СМК.
Указанные подгруппы различались между собой по дооперационным показателям радионуклидной ангиопульмоно- и томовентрикулографии. Так, в первой подгруппе пациентов (с удовлетворительной функцией правого желудочка) значения КДО ЛЖ, КСО ЛЖ, Т1/2ПЖ, ТПСЛ, ТАМН были достоверно меньшими, а ФВ ЛЖ, УО ПЖ, ФВ ПЖ, МСИ ПЖ, МСН ПЖ, ССН/3 ПЖ, ТПР – большими, по сравнению с аналогичными значениями во второй подгруппе (со сниженной сократительной функцией ПЖ).
В результате проведения множественного регрессионного анализа (рис. 2) установлено, что значения фракции выброса ПЖ после коррекции порока могут быть спрогнозированы по предоперационным значениям фракции выброса, ударного объема и максимальной скорости изгнания РФП из правого желудочка. Уравнение множественной линейной регрессии в данном конкретном случае имеет вид:
ФВПЖ п/о = 20,7 – 0,55 × УОПЖ д/о + 1,11 × ФВПЖ д/о – 1,21 × МСИПЖ д/о
где ФВПЖ п/о – фракция выброса правого желудочка после коррекции стеноза МК;
УОПЖ д/о – ударный объем правого желудочка до коррекции стеноза МК;
ФВПЖ д/о – фракция выброса правого желудочка до коррекции стеноза МК;
МСИПЖ д/о – максимальная скорость изгнания правого желудочка до коррекции стеноза МК.
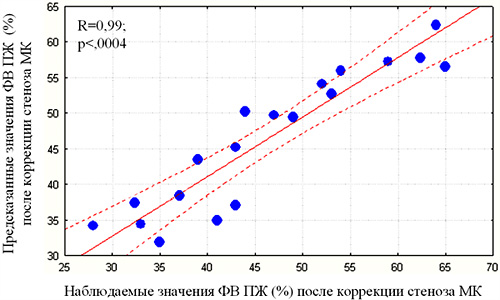
Рисунок 2. График, отражающий корреляцию, между фактически наблюдаемыми и предсказанными (согласно уравнению множественной линейной регрессии) послеоперационными значениями ФВПЖ.
Заключение
Использование радионуклидной ангиопульмонографии и томовентрикулографии позволяет количественно и визуально объективизировать нарушения легочной микроциркуляции и региональной сократимости желудочков сердца. При этом качество изображения и точность вычисления параметров гемодинамики не зависят от особенностей геометрии желудочков и экранирующих их структур (грудина, ребра, легкие, послеоперационные изменения мягких тканей и т.д.).
Обусловленные стенозом митрального клапана изменения гемодинамики правого желудочка в наибольшей степени проявляются снижением ударного объема, фракции выброса, максимальной скорости изгнания и средней скорости наполнения, а также увеличением конечно-систолического объема. Кроме того, наличие стеноза МК проявляется замедлением легочного кровотока. После коррекции порока в наибольшей степени нормализуются конечно-систолический объем, фракция выброса, максимальная скорость изгнания правого желудочка, размеры правого предсердия и скоростные показатели малого круга кровообращения.
Выполнение равновесной томовентрикулографии при митральном стенозе позволяет прогнозировать состояние сократимости ПЖ после оперативной коррекции митрального стеноза.
Благодаря указанным особенностям методы радионуклидной ангиопульмонографии и томовентрикулографии могут быть использованы для комплексной неинвазивной оценки функционального состояния МКК и прогноза нормализации функционального состояния правых отделов сердца пациентов со стенозом митрального клапана.
Литература
- Iung B., Baron G., Butchart E.G. et al. A prospective survey of patients with valvular heart disease in Europe: The Euro Heart Survey on Valvular Heart Disease. Eur Heart J. 2003 Jul; 24(13): 1231-43.
- Pomerantzeff P.M., Brandão C.M., Leite Filho O.A. et al. Mitral valve repair in rheumatic patients with mitral insuficiency: twenty years of techniques and results. Rev Bras Cir Cardiovasc. 2009 Dec; 24(4): 485-9.
- Бураковский В.И., Бокерия Л.А. Сердечно-сосудистая хирургия. 2-е изд. доп. М.: Медицина, 1996. 767 с.
- Groote de P., Millaire A., Foucher-Hossien C. et al. Right ventricular ejection fraction is an independent predictor of survival in patients with moderate heart failure. J Am Coll Cardiol 1998; 32: 948-954.
- Pande S., Agarwal S.K., Dhir U. et al. Pulmonary arterial hypertension in rheumatic mitral stenosis: does it affect right ventricular function and outcome after mitral valve replacement? Interact Cardiovasc Thorac Surg. 2009 Sep; 9(3): 421-5. Epub 2009 Jun 4.
- Haddad F., Hunt S.A., Rosenthal D.N. et al. Right ventricular function in cardiovascular disease, part I: Anatomy, physiology, aging, and functional assessment of the right ventricle. Circulation. 2008 Mar 18; 117(11): 1436-48.
- Tugcu A., Yildirimtürk O., Tayyareci Y. at al. Evaluation of subclinical right ventricular dysfunction in obstructive sleep apnea patients using velocity vector imaging. Circ J. 2010 Feb; 74(2): 312-9. Epub 2009 Dec 15.
- Шиллер Н., Осипов М.А. Клиническая эхокардиография. М.: Практика, 1993. 347 с.
- Miller S., Reissen R., Claussen C. et al. Cardiac Imaging ISBN 160406014X, 9781604060140 Thieme, 2007.
- Schmidt M., Crnac J., Dederichs B. et al. Magnetic resonance imaging in valvular heart disease. Int J Card Imaging. 1997 Jun; 13(3): 219-31.
- Стасев А.Н. Комбинированное лечение фибрилляции предсердий при митральном пороке сердца. Сибирский медицинский журнал, 2010. Том 25, №2, Выпуск 2, С.38-42.
- Alfakih K., Plein S., Thiele H. Et al. Normal human left and right ventricular dimensions for MRI as assessed by turbo gradient echo and steady-state free precession imaging sequences. J Magn Reson Imaging. 2003 Mar; 17(3): 323-9.
- Сиваченко Т.П., Белоус А.К., Зозуля А.А. Радиокардиография. Киев: Здоровье, 1984. 144 с.
- Dollery C.T., West J.B., Wilcken D.E.L. et al: Regional pulmonary blood flow in patients with circulatory shunts. Br. Heart J. 1961; 23:225.
