Опыт клинического применения магнитно-резонансной ангиографии
Е.А. Богoлепова**, Е.В. Нетесова**, Г.Э. Шустрова***, В.Г. Абалмасов*
* ДГОУ Институт повышения квалификации ФМБА России
** Федеральный медицинский центр им. Бурназяна ФМБА России
*** Клиническая больница № 38 ФМБА России
РЕФЕРАТ: Проанализирован опыт использования различных методик магнитно-резонансного исследования артериального и венозного отделов сосудистого русла головы и шеи, и показана возможность одномоментного контрастного исследования брахиоцефальных сосудов.
КЛЮЧЕВЫЕ СЛОВА: магнитно-резонансная артериография, магнитно-резонансная венография.
Анализ структуры смертности в России показывает, что основной удельный вес составляет смертность от болезней системы кровообращения – 56,5%, из них 27,5% приходится на ишемическую болезнь сердца, 20,2% – на цереброваскулярные заболевания [1]. О высокой медицинской и социальной значимости сосудистых заболеваний мозга свидетельствуют также следующие данные: в острой стадии заболевания погибают 27-32% больных инсультом, в течение первого года умирают более половины больных (52-63%), и к пяти годам умирают 70% больных, перенесших первичный инсульт [2].
Не менее серьезную проблему представляют собой и хронические сосудистые заболевания (в отечественной литературе чаще встречается термин «дисциркуляторная энцефалопатия»), отличающиеся от острых нарушений мозгового кровообращения постепенным медленным или ступенеобразным нарастанием неврологической симптоматики [3]. В развитии хронической ишемии мозга и нарушения микроциркуляции имеют значение такие факторы, как затруднение венозного оттока [4], повышение агрегационных свойств тромбоцитов и эритроцитов, снижение деформируемости эритроцитов [5].
Выраженность симптоматики у больных с церебральными сосудистыми заболеваниями, длительная утрата трудоспособности, высокий уровень стойкой инвалидизации и смертности определяют преимущественное внимание исследователей именно к артериальному отделу мозгового сосудистого русла. В то же время, очевидная взаимосвязь артериального и венозного кровообращения мозга (даже с учетом преобладания значимости первого) диктует необходимость корректной анатомически и физиологически объективной оценки состояния путей венозного оттока. В последнее время в связи с развитием магнитно-резонансных и ультразвуковых технологий все большее внимание направлено на оценку венозного отрезка сосудистого русла и артерио-венозных взаимоотношений [6-12].
Высокая значимость анатомической замкнутости Виллизиева круга хорошо известна. Варианты строения с отсутствием целостности ухудшают прогноз заболевания в случае развития острого нарушения мозгового кровообращения, увеличивают количество осложнений при проведении реконструктивных операций на сонных артериях [13-16]. При этом по-прежнему недостаточно данных об анатомических и физиологических особенностях венозного оттока, клиническая значимость которых до сих пор не ясна, но может оказаться весьма существенной.
Материалы и методы
Магнитно-резонансная ангиография выполнена у 178 пациентов с различной выраженностью поражения церебрального артериального русла, находившихся на обследовании и лечении в Федеральном медицинском биофизическом центре им. А.И. Бурназяна ФМБА России. Из них 82 женщины и 96 мужчин в возрасте от 29 до 82 лет, средний возраст составил 58,1±4,2 года.
Исследование головного мозга и церебральных сосудов осуществлялось на высокопольном магнитно-резонансном томографе Magnetom Symphony (Siеmens) с напряженностью магнитного поля 1,5 Т. Высокопроизводительные градиенты (40 мТл/м со скоростью нарастания 200 Тл/м/сек по каждой из x, y, z осей), циркулярно-поляризованная технология мультиэлементных радиочастотных катушек, объединенных в единый виртуальный массив для их панорамного использования.
Преимущества и недостатки различных методик исследования
Наиболее важными условиями корректной оценки состояния сосудистого русла являются получение адекватного сигнала от потока крови (то есть коррелирующего со скоростью потока, а не с взаимоотношением направления тока крови и плоскости градиентного поля), а также хорошее пространственное разрешение (учитывая разветвленность и богатство анастомозов церебральной сосудистой сети). Несколько примеров представлено на рисунках 1-5.
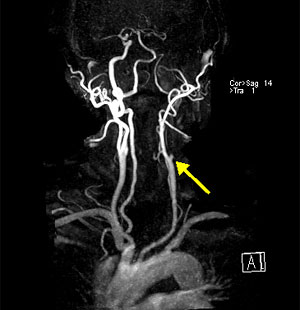
Рисунок 1. 3D время-пролетная ангиография.
Окклюзия внутренней сонной артерии слева (стрелка).

Рисунок 2. 2D время-пролетная ангиография экстракраниальных артерий,
затруднена оценка начальных отделов, коронарная проекция.

Рисунок 3. 2D время-пролетная ангиография экстракраниальных вен.
Выраженная неравномерность сигнала, вплоть до его исчезновения,
что делает невозможным корректное заключение по данному снимку.

Рисунок 4. 3D время-пролетная ангиография экстракраниальных вен.
Менее выраженная неравномерность сигнала. При этом для получения качественного снимка
необходимо ограничить поле исследования.

Рисунок 5. Фазово-контрастная ангиография экстракраниальных вен.
Неравномерность сигнала, при этом сохраняется диагностическое качество снимка для вен,
для получения которого также необходимо оганичить поле исследования.
Основные преимущества время-пролетного бесконтрастного исследования заключаются в том, что при высоком пространственном разрешении и высоком соотношении сигнал/шум мы получаем хорошее диагностическое качество изображений артериального русла как на экстра-, так и на интракраниальном уровне. На проведение исследования требуется относительно небольшое время. При этом следует отметить низкую чувствительность методики к медленному кровотоку, то есть существуют практические трудности оценки состояния венозного русла. Основным недостатком методик время-пролетной ангиографии является плохая визуализация сосудов в области изгибов, особенно при углах, приближающихся к 90°. Связано это с потерей ламинарного характера кровотока и образованием турбулентности в области поворотов и изгибов сосудов. Поэтому оценка ангиографических изображений в TOF-последовательностях всегда следует проводить с учетом этих факторов.
Основным преимуществом фазово-контрастной ангиографии бесспорно является высокая чувствительность к медленному кровотоку, поскольку существует возможность произвольной настройки в зависимости от предполагаемой скорости кровотока. При известных параметрах градиентного поля (величина и время воздействия) можно также определить такой функциональный показатель, как собственно скорость кровотока. При анализе ангиограмм следует помнить следующее: если реальная скорость кровотока превысит заданную максимальную величину скорости кровотока в исследуемом объеме, это вызовет появление артефактов наложения на окончательном изображении.
К основным недостаткам методики традиционно относится большая длительность проведения исследования, хотя современное программное сопровождение помогает существенно снизить этот недостаток. Кроме того, относительно низкое соотношение сигнал/шум. Так, например, попытка уменьшить время получения ангиограмм на экстракраниальном уровне за счет уменьшения поля обзора в направлении обратной свертки (rectangular FOV – rFOV) сразу приводит к снижению соотношения сигнал/шум. При этом остаются серьезные трудности с получением магнитно-резонансных венограмм значительной протяженности.
Как показал наш опыт использования различных методик магнитно-резонансной ангиографии, существуют определенные сложности интерпретации венограмм при выполнении стандартных протоколов исследования, например, ограничение получения качественного изображения при время-пролетной и фазово-контрастной ангиографии из-за неравномерности кровотока, то есть сложно получить равномерный сигнал от крови, что затрудняет оценку кровотока в целом.
Большинство проблем, с которыми нам пришлось столкнуться, совпадают с мнением исследователей о проблемах интерпретации магнитно-резонансной венографии [17-20].
Сегодня уже не обсуждается вопрос о существенном улучшении качества магнитно-резонансных ангиограмм при применении контрастных веществ, тем более что современные контрасты на основе гадолиния являются практически безопасными. Возможности МРА с контрастным усилением в большей степени основаны на сокращении времени T1-релаксации, нежели другие эффекты время-пролетной или фазово-контрастной методик. Безусловно, положительным моментом является высокая чувствительность к медленному кровотоку, что важно для исследования венозного русла. Величина задержки между введением болюса контрастного вещества и появлением его в зоне интереса зависит от скорости кровотока, величины сердечного выброса и протяженности сосудистого русла от сердца.
Для улучшения качества визуализации венозной фазы исследования на экстракраниальном уровне нами использованы одновременно две катушки – головная и для шеи (рис. 6).

Рисунок 6. Общий вид при исследовании пациента с использованием двух катушек.
Протокол исследования включал обязательное проведение традиционной МР томографии головного мозга с использованием сверхбыстрых последовательностей спинового эха в аксиальной, коронарной и сагиттальной плоскостях. Анализировали Т1- и Т2-взвешенные изображения, а также в режиме инверсионного восстановления с подавлением сигнала от жидкости (Fluid Attenuated Inversion Recovery – FLAIR). Анализировали состояние головного мозга, желудочковой системы, размеры ликворосодержащих пространств и их симметричность. Первичная оценка состояния интракраниального артериального русла и Виллизиева круга проводилась с помощью бесконтрастной время-пролетной методики 3D multi-slab. Затем болюсно через локтевую вену вводился контраст со скоростью 3 мл/с из расчета 0,2 мл на килограмм. В качестве контрастного вещества использовались препараты гадолиния. При появлении контраста в дуге аорты включался режим ангиографии. Далее через 26 секунд оценивались изображения артериальной фазы, через следующие 26 секунд оценивали состояние интракраниального и экстракраниального венозного русла, через следующие 26 секунд – повторная оценка венозного русла на интра- и экстракраниальном уровне (у пожилых пациентов или у пациентов с предполагаемым снижением скорости кровотока).
Обязательным условием проведения исследования является направленность свертки против тока крови, то есть при артериографии – кранио-каудальное направление, при венографии – обратное (рис. 7-9).
В целом протокол контрастной магнитно-резонансной ангиографии аналогичен протоколам, применяемым в трехмерной время-пролетной ангиографии. Мы также использовали трехмерную градиентную импульсную последовательность. Для подавления сигнала от неподвижных тканей выбирается короткое время повторения (TR) и относительно большой (по сравнению с бесконтрастной методикой – из-за слишком быстрого насыщения крови) угол отклонения (FA). Опытным путем нами были подобраны следующие параметры протокола: исследование проводилось в коронарной плоскости при следующих условиях: FOV – 400 мм, Slice thickness – 1,4 мм, TR – 3,33 мс, TE – 1,15 мс. Количество срезов – 96 в блоке. Время проведения полного исследования (включая исследование головного мозга) не превышало, как правило, 14 минут.

Рисунок 7. Ангиография с контрастированием. Артериальная фаза исследования.

Рисунок 8. Ангиография с контрастированием. Венозная фаза исследования, первые 26 секунд.

Рисунок 9. Ангиография с контрастированием. Венозная фаза исследования, вторые 26 секунд. Кроме визуализации основных синусов, визуализируются пути оттока на уровне шеи, вплоть до слияния плечеголовных вен.
Определенные сложности при интерпретации результатов могут возникать при недостаточном расширении поля сбора информации (рис. 10, 11).

Рисунок 10. Дефект контрастирования верхнего сагиттального синуса (стрелка)
связан с недостаточным расширением информационного блока.
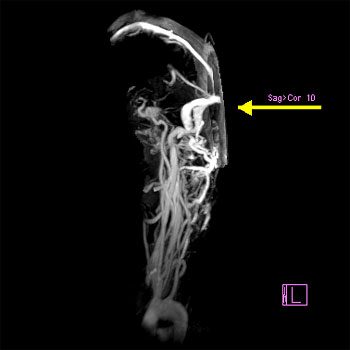
Рисунок 11. На данном снимке представлен результат
недостаточной ширины захвата изображения (стрелка).
На представленных рисунках хорошо видны дефекты заполнения синусов, связанные с техническими ошибками получения изображения. Плоскость ограничения четко видна при ротации трехмерного снимка.
Эффект наслоения сосудистых изображений венозной фазы исследования разрешается, как правило, при оценке пространственного трехмерного взаимоотношения артерий и вен (рис. 12).

Рисунок 12. Пространственные взаимоотношения артерий и вен
при проведении одномоментного контрастного исследования.
Сложности интерпретации результатов возникали, как правило, при недостаточном расширении поля сбора информации, поэтому исходно следует выставлять максимальную ширину блока. Эффект наслоения сосудистых изображений венозной фазы исследования разрешается, как правило, при оценке пространственного взаимоотношения артерий и вен.
Таким образом, использование контрастного вещества, корректное применение свертки против направления тока крови, трехмерная реконструкция сосудистого русла делают возможным дополнение стандартного исследования головного мозга оценкой артериального и венозного русла на интра- и экстракраниальном уровне без значительного увеличения времени процедуры.
В заключение следует отметить широкий спектр клинического применения магнитно-резонансной ангиографии. При этом возможности методики предполагают практически неограниченные варианты конфигурации протокола исследования в зависимости от задач, определяющих диагностическую направленность исследования.
Литература
- Суслина З.А., Варакин Ю.Я., Верещагин Н.В. Сосудистые заболевания головного мозга. М. «МЕДпресс-информ», 2009. 350 с.
- Виленский Б.С. Современная тактика борьбы с инсультом. СПб., Фолиант, 2005. 284 с.
- Кадыков А.С., Манвелов Л.С., Шахпаронова Н.В. Хронические сосудистые заболевания головного мозга (дисциркуляторная энцефалопатия). М., Гоэтар-Медиа, 2006. 222 с.
- Машин В.В., Кадыков А.С. Гипертоническая энцефалопатия. Клиника и патогенез. Ульяновск: УлГУ. 2002. 139 с.
- Ионова В.Г., Суслина З.А. Реологические свойства крови при ишемических нарушениях мозгового кровообращения. Неврологический журнал. 2002. Т.7. №3. С.4-9.
- Тулупов А.А. Возможности магнитно-резонансной томографии в морфо-функциональной оценке церебрального венозного кровотока и ликвороциркуляции. Автореф. дис. докт. мед. наук. Томск. 2011. 45 с.
- Белова Л.А. Гипертоническая энцефалопатия: роль артерио-венозных взаимоотношений в формировании ее клинико-патогенетических подтипов. Автореф. дис. докт. мед. наук. Москва. 2011. 41 с.
- Бурдин С.Н. Оценка гемодинамической значимости обструкции внутренних яремных вен неинвазивными и малоинвазивными методами лучевой диагностики: дис. канд. мед. наук. Томск. 2008. 149 с.
- Дическул М.Л., Куликов В.П., Маслова И.В. Ультразвуковая характеристика венозного оттока по позвоночным венам. Ультразвуковая и функциональная диагностика. 2008. №4. С.33-40.
- Золотухина Н.Е., Машин В.Вл., Фонякин Ф.В. и др. Состояние венозного оттока из полости черепа у больных гипертонической энцефалопатией с хронической сердечной недостаточностью. Неврологический вестник. 2006. Т.38. Вып. 3-4. С.5-9.
- Синицын В.Е., Терновой С.К., Стукалова О.В., Тимонина Е.А. Магнитно-резонансная флебография. Визуализ. в клинике. 1997. №11, С.6-9.
- Лелюк В.Г, Лелюк С.Э. Критерии оценки экстрацеребрального венозного кровообращения в норме по данным дуплексного сканирования. Ультразвуковая диагностика. 1999. №2. С.37-44.
- Корниенко В.Н., Пронин И.Н., Арутюнов Н.В. и др. МР-ангиография с применением нового одномолярного контрастного препарата «Гадовист 1.0» в нейрохирургической клинике. Медицинская визуализация. 2004. №1. С.16-25.
- Шахнович А.Р., Шахнович В.А. Диагностика нарушений мозгового кровообращения: транскраниальная допплерография. Москва, 1996. 436 с.
- Шуракова А.Б. Возможности оптимизированной методики фазовоконтрастной магнитно-резонансной ангиографии при хирургическом лечении больных с поражением сонных артерий: автореф. дис. канд. мед. наук. М.: 2009. 30 с.
- Kamarioti E., Maniatis V., Papadopoulos A. et al. КТ-ангиография виллизиева круга в диагностике острой церебральной ишемии. Медицинская визуализация. 2001. №4. С.22-29.
- Бурдин С.Н. Оценка гемодинамической значимости обструкции внутренних яремных вен неинвазивными и малоинвазимными методами лучевой диагностики: дис. канд. мед. наук. Томск. 2008. 149 с.
- Семенов С.Е. Магнитно-резонансная венография в диагностике компрессионных поражений брахиоцефальных вен: дис. канд. мед. наук. Томск, 1999. 138 с.
- Alper F., Kantarci M., Dane S. et al. Importance of Anatomical Asymmetries of Transverse Sinuses: An MR Venographic Study. Cerebrovasc Dis. 2004. V.18. P.236-239.
- Leach J.L., Fortuna R.B., Jones B.V., Gaskill-Shipley M.F. Imaging of Cerebral Venous Thrombosis: Current Techniques, Spectrum of Findings, and Diagnostic Pitfalls. RadioGraphics. 2006. V.26. Special Issue. P.19-42.
